Blog
Nitrogênio Amoniacal em Água e Efluentes
Nitrogênio amoniacal,água e efluentes
Em águas e
águas residuais, as formas de nitrogênio de maior interesse são, em ordem
decrescente de estado de oxidação: nitrato, nitrito, amônia, e nitrogênio
orgânico. Todas estas formas de nitrogênio, bem como o gás nitrogênio (N2),
são bioquimicamente sujeitos a mudanças e são componentes do ciclo do
nitrogênio.
A amônia está
presente naturalmente nos corpos d'água como produto da degradação de compostos
orgânicos e inorgânicos do solo e da água, resultado da excreção da biota,
redução do nitrogênio gasoso da água por microrganismos ou por trocas gasosas
com a atmosfera. A amônia é, também, constituinte comum no esgoto sanitário,
resultado direto de descargas de efluentes domésticos e industriais, da
hidrólise da ureia e da degradação biológica de aminoácidos e outros compostos
orgânicos nitrogenados.
TOXICIDADE
Nas soluções
aquosas, a amônia pode se apresentar sob a forma ionizada (NH4+)
ou não-ionizada (NH3) de acordo com o pH, sendo estas formas
intercambiáveis cuja a soma se constitui a amônia total ou nitrogênio amoniacal
total. Ambas as formas são prejudiciais para a biota aquática, entretanto, a
forma não ionizada é mais tóxica quando comparada a forma ionizada. Este fato
está relacionado à sua permeabilidade através da membrana celular dos peixes e
pequenos vertebrados presentes e de sua solubilidade em lipídios que nestes
ocasionam efeitos letais em rios. Além
disso, a amônia pode se ligar a metais pesados, formando complexos considerados
tóxicos.
Os seres humanos e os animais superiores são menos sensíveis a amônia na água, porém a ingestão prolongada de água contendo mais de 1 mg/L (ppm) de amônia pode ser prejudicial ao organismo. Soluções com concentrações superiores a 1000 mg/L (ppm) podem causar queimaduras graves e cicatrizes de pele sensível e membranas mucosas.
MÉTODO DE DETERMINAÇÃO:
DESTILAÇÃO PRELIMINAR + TITULAÇÃO
A concentração de amônia e a presença de interferentes são os dois principais fatores que influenciam a seleção do método de determinação. Em geral, a determinação manual direta de baixas concentrações de amônia está confinada às águas potáveis, superfície limpa ou águas subterrâneas, e efluentes de águas residuais nitrificadas de boa qualidade. Em outros casos e onde haja interferências é necessária uma etapa preliminar de destilação.
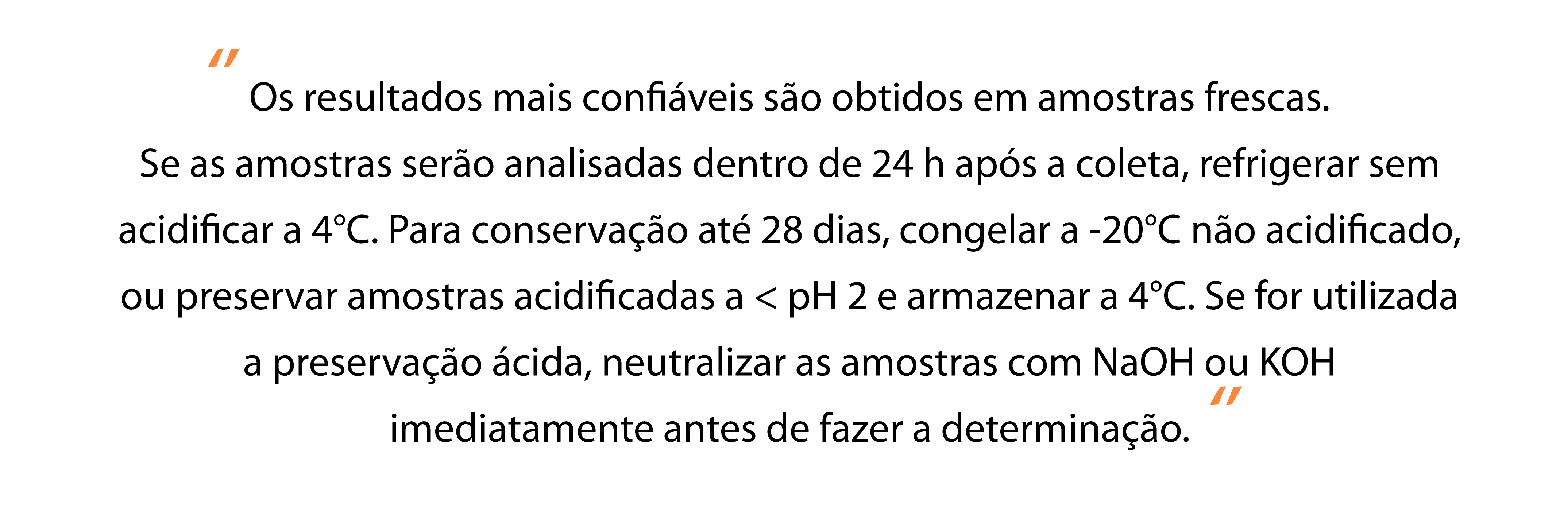

Câmara fria com controle de temperatura, modelo TE-4030/1, incubadora, modelo TE-371/240L,
câmara de conservação, modelo TE-385
Essa nota de
aplicação se refere ao procedimento de destilação e titulação, utilizado
especialmente para concentrações de NH3-N superiores a 5 mg/L, onde a
amostra é destilada, tratada com ácido bórico e titulada com solução de H2SO4.
O término da titulação se dá quando há a mudança de coloração da solução para
lilás/lavanda pálida.
A amostra é
tamponada a pH 9,5 com um tampão de borato para diminuir a hidrólise de
cianatos e compostos orgânicos de nitrogênio e destilado em uma solução de
ácido bórico, sendo a amônia determinada por titulação com uma solução padrão de
H2SO4.
- Para amostras de lodo ou sedimentos: Pesar rapidamente cerca de
1% de amostra úmida, equivalente a aproximadamente 1 g de peso seco, em um
frasco ou cadinho de pesagem. Lavar a amostra em um balão de 500 mL com água e
diluir até 250 mL. Proceder a destilação, mas adicionar um pedaço de cera de
parafina ao frasco de destilação e recolher apenas 100 mL de destilado.
PROCEDIMENTO
1. Homogeneizar a amostra
2. Retirar uma alíquota representativa em relação a quantidade de
nitrogênio amoniacal presente na amostra de acordo com a tabela 1, e transferir
para um béquer. Amostras com concentração superior, devem ser diluídas.
Tabela 1. Parâmetros para definição do volume de amostra e tipo de frasco utilizado.
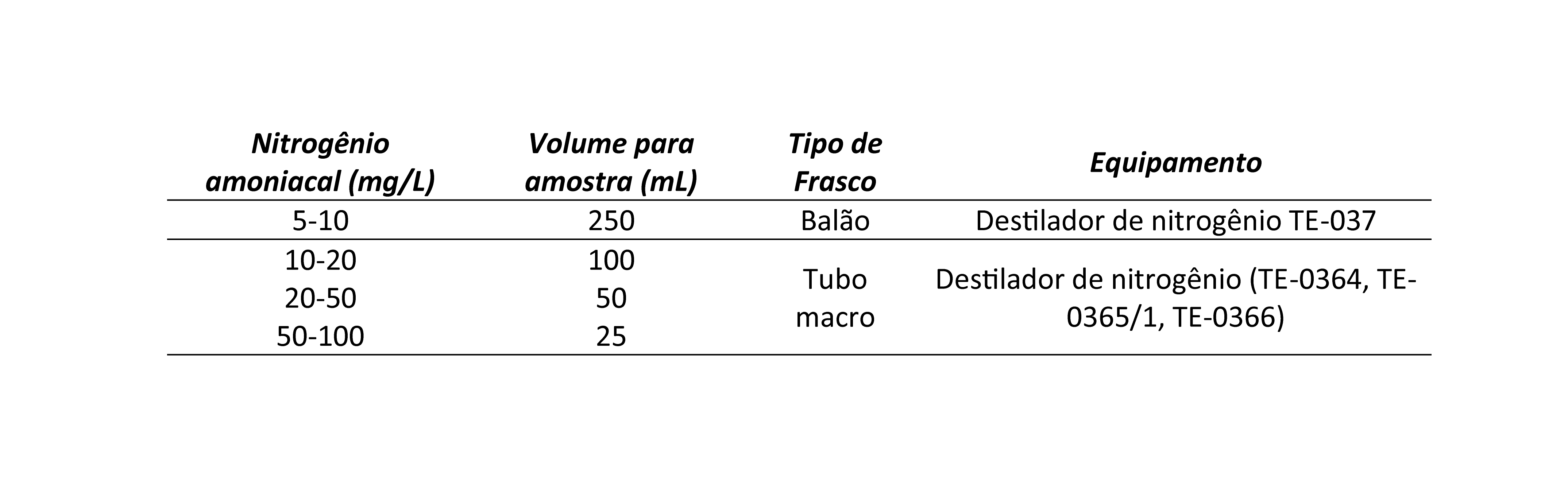
3.Adicionar 25mL de Solução Tampão de Borato
4. Ajustar o pH para 9,5 com Hidróxido de Sódio 6N
5. Reservar
6. Adicionar 50mL de Solução Absorvente de Ácido Bórico num balão
volumétrico de 250mL
7. Transferir a amostra preparada e reservada para o frasco selecionado
de acordo com a tabela 1
8. Conectar o frasco ao destilador
9. Destilar a uma taxa de 6
a 10 mL/min
10. Acoplar um erlenmeyer de 250mL contendo 50 ml de solução de
Ácido Bórico na saída do destilado, de modo que a mangueira de saída esteja
submersa na solução
11. Coletar no mínimo 200 ml de destilado (para lodo ou sedimento,
coletar apenas 100 ml)
12. Transferir o conteúdo para um béquer de 600mL
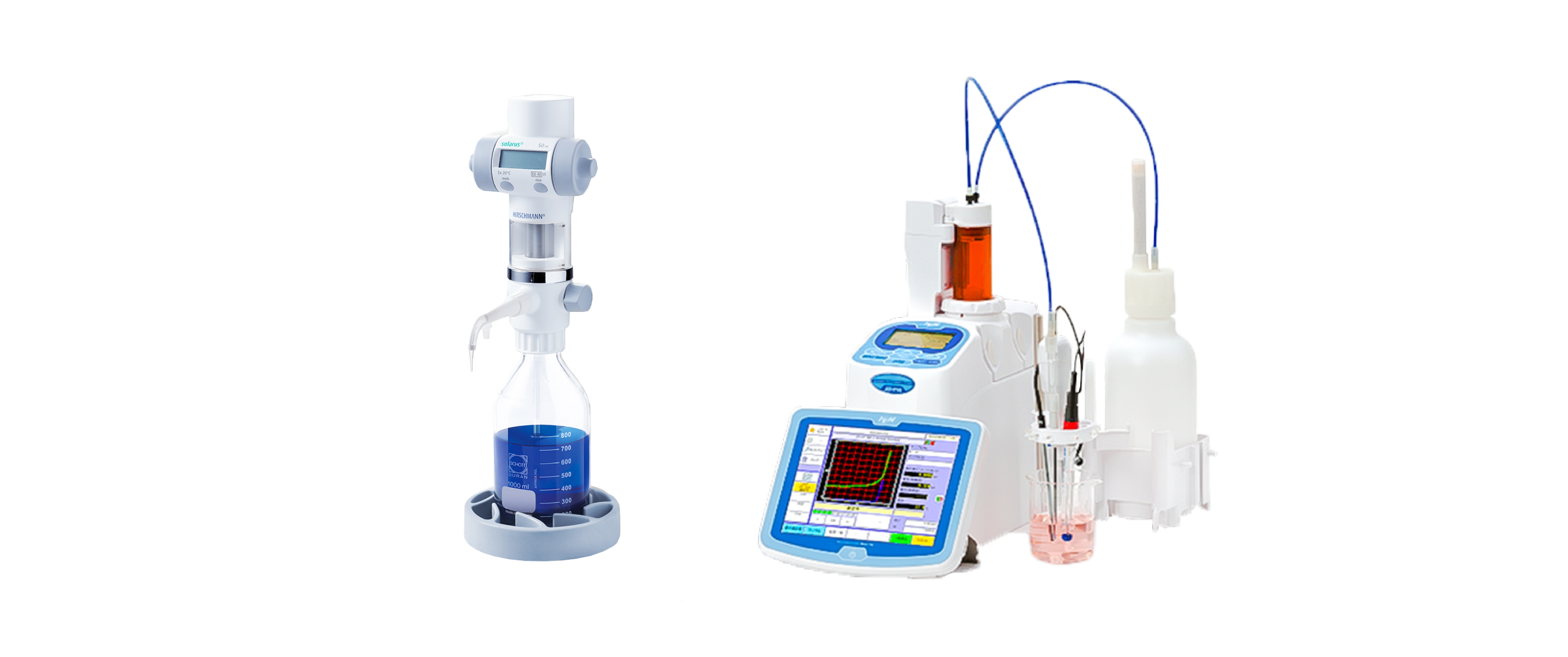
13. Efetuar a titulação da amônia no destilado com solução padrão titulante de H2SO4 (0;02N) até ocorrer mudança de cor para lavanda pálida. Para a titulação pode ser utilizado uma bureta digital ou titulador potenciométrico automático.
14. Fazer um branco em todas as etapas do procedimento e aplicar a
correção necessária aos resultados.
CÁLCULO:
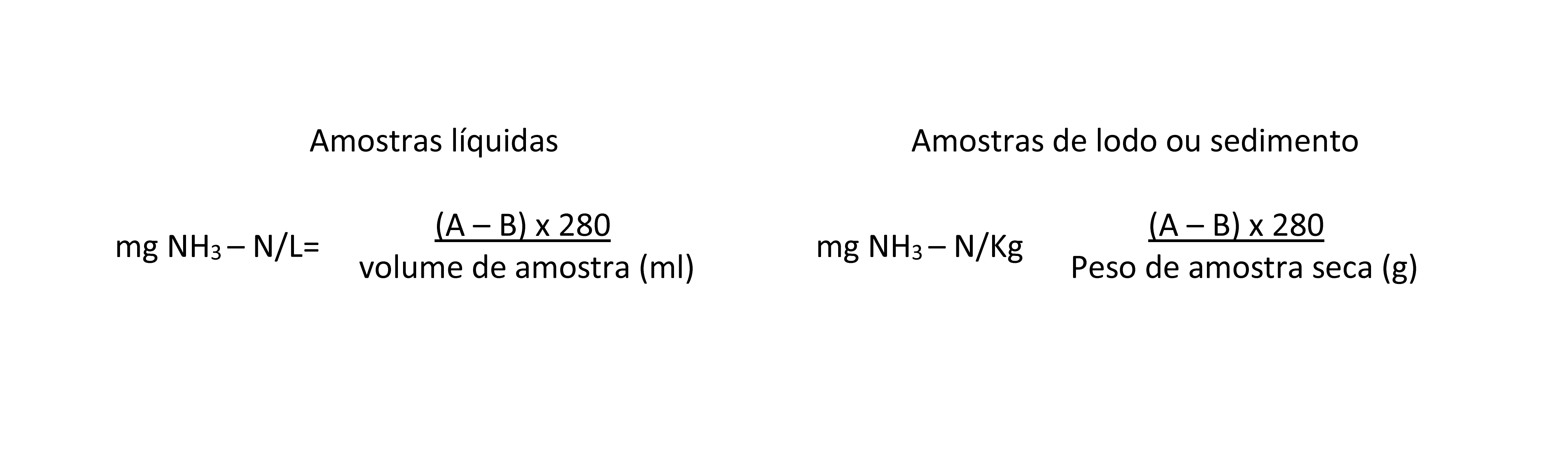
Onde, A= Volume (mL) de H2SO4 titulado para amostra
e B= Volume (mL) de H2SO4 titulado para o branco.
A água utilizada para o preparo de soluções utilizados em análises laboratoriais deve ser livre de impurezas orgânicas e inorgânicas para garantir resultados precisos e reprodutíveis. Para obter água de qualidade devem ser utilizados equipamentos como destiladores de água ou osmose reversa. Saiba mais sobre TRATAMENTO E FILTRAGEM DA ÁGUA PARA ANÁLISES LABORATORIAIS no artigo em nosso blog.

CONSIDERAÇÕES FINAIS
Os compostos
de nitrogênio presente em águas e efluentes são prejudiciais ao meio-ambiente,
impactando a vida de organismos aquáticos além de se constituir um risco também
a saúde humana. A amônia é a forma mais comum em que o nitrogênio é encontrado
em efluentes oriundos de esgotos domésticos brutos (VON SPERLING, 2002), sendo
um parâmetro físico-químico importante a ser analisado. Ressalta-se a
importância de avaliar a concentração de amônia esperada na amostra e a
presença de interferentes, para assim selecionar a metodologia adequada e
garantir resultados satisfatórios.
A
concentração de amônia permitida em águas potáveis assim como os padrões de
lançamento de efluentes de fontes de poluição em corpos hídricos variam de
acordo com a legislação ambiental de cada país. No Brasil a resolução 430/2011
do Conselho Nacional do Meio Ambiente (CONAMA), que dispõe sobre as condições e
padrões de lançamento de efluentes, determina que o limite máximo de nitrogênio
amoniacal total em lançamentos é de 20,0 mg/L.
SOLUÇÕES UTILIZADAS:
Solução tampão de borato: Adicionar 88 mL de solução de NaOH 0,1N
a 500 mL aproximadamente de solução de tetraborato de sódio 0,025M (Na2B4O7)
(9,5 g de Na2B4O7 • 10 H2O/L) e diluir a 1 L.
Solução de indicador misto: Dissolver 200 mg de indicador vermelho
de metila em 100 mL de álcool etílico 95% ou isopropílico. Dissolver 100 mg de
azul de metileno em 50 mL de álcool etílico 95% ou álcool isopropílico. Combinar soluções. Preparar mensalmente.
SOBRE A TECNAL
A Tecnal tem como missão contribuir para o desenvolvimento científico, tecnológico e com a indústria nacional e internacional por meio da fabricação e da comercialização de equipamentos científicos, da prestação serviços especializados e da disseminação do conhecimento.
A empresa busca crescer de maneira inovadora e sustentável, focada na continuidade e na excelência operacional, de forma a tornar-se uma referência no mercado brasileiro e internacional de equipamentos científicos. Fale conosco: pelo Telefone/WhatsApp (19) 2105-6161, e-mail contato@tecnal.com.br ou pelo site clicando aqui.
REFERÊNCIAS
APHA, Standard
Methods for the Examination of Water and Wastewater. E.W.
Rice, R.B. Baird, A.D. Eaton, L.S. Clesceri, editors. 23ª ed. Washington: American Public
Health Association, 2017. 1496p.
Brasil. Ministério do Meio Ambiente. CONAMA. Resolução nº 430, de
13 de maio de 2011. Dispõe sobre as condições e padrões de lançamento de
efluentes, complementa e altera a Resolução no 357, de 17 de março de 2005, do
Conselho Nacional do Meio Ambiente.
Von Sperling, M. Lodos ativados. v. 4. Belo Horizonte: Departamento de Engenharia Sanitária e Ambiental; Universidade Federal de Minas Gerais, 2002. 428 p



